Автор: Красен Парушев
Афилиация: Хипербарен център „Барокамери Парушев“, Бургас, България.
Резюме
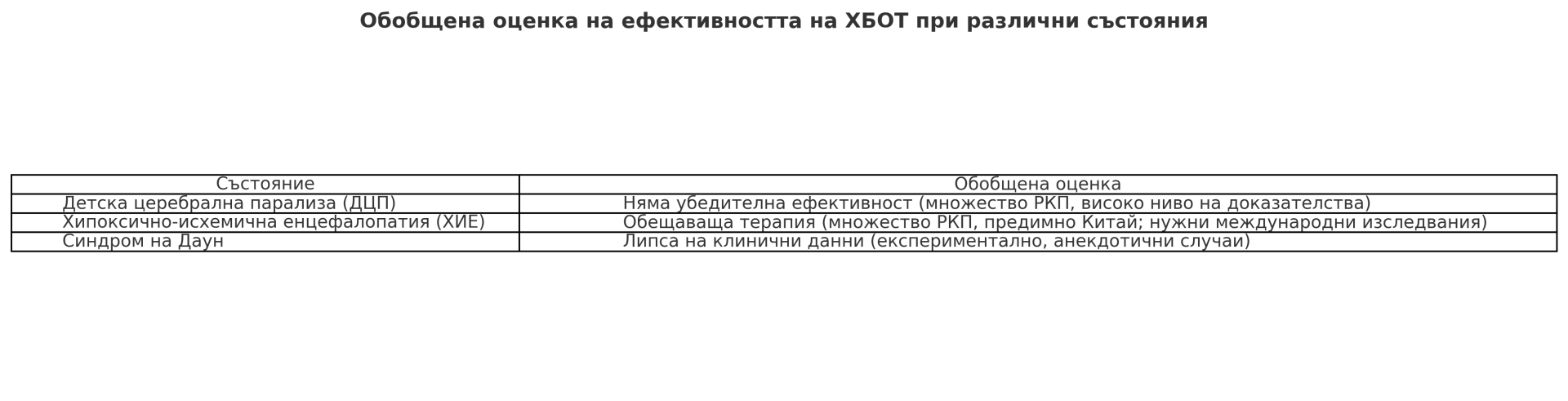
Цел: Настоящият обзор представя задълбочен преглед на научните данни относно ефектите и безопасността на хипербарната кислородна терапия (ХБОТ) при три педиатрични състояния – детска церебрална парализа (ДЦП), неонатална хипоксично-исхемична енцефалопатия (ХИЕ) и синдром на Даун.
Методи: Проведен е систематизиран литературен преглед на публикации от последните 10–15 години, включително рецензирани клинични проучвания, систематични обзори и мета-анализи. Търсенето обхваща бази данни като PubMed, Cochrane Library и др., като са включени главно изследвания с високо ниво на доказателственост (напр. рандомизирани контролирани проучвания – РКП, мета-анализи). Оценена е качеството на доказателствата и са отбелязани нивата на доказателственост.
Резултати: При ДЦП множествените РКП не показват статистически значимо подобрение в моторните или когнитивните функции на децата, подложени на ХБОТ, спрямо контролни групи (включително контрол с нагнетен въздух или стандартна рехабилитация) . Съществуват висококачествени доказателства, че ХБОТ не води до трайно подобрение на функционалното състояние при ДЦП . Нещо повече, умерено ниво на доказателства сочи по-висока честота на нежелани ефекти (напр. баротравма на средното ухо) при ХБОТ в сравнение с контрол . За неонаталната ХИЕ, обширни данни основно от Китай предполагат, че добавянето на ХБОТ към стандартното лечение може да подобри неврологичния изход и да намали риска от неврологични усложнения . Мета-анализ на 46 РКП с 4199 новородени отчита значимо повишаване на показателя за “обща ефективност” на лечението и по-ниска честота на неврологични усложнения в групите с ХБОТ . Въпреки това, тези проучвания са с хетерогенни протоколи и ограничени географски (главно Китай), поради което резултатите трябва да се интерпретират с повишено внимание . При синдром на Даун данните са оскъдни – липсват големи контролирани проучвания. Налични са само казуистични съобщения и непубликувани клинични наблюдения, според които ХБОТ може да подобри когнитивните функции или общото състояние при някои деца, но научни доказателства за това твърдение засега няма. Физиологични изследвания показват, че лицата със синдром на Даун имат признаци на хронична тъканна хипоксия , което предоставя теоретична обосновка за потенциална полза от ХБОТ, но клинично това остава недоказано.
Заключение: ХБОТ е утвърдена терапия за ограничен брой показания в медицината, но приложението ѝ при ДЦП, ХИЕ и синдром на Даун остава контроверсно. При ДЦП наличните висококачествени доказателства не подкрепят рутинното използване на ХБОТ за подобряване на моторното развитие или когницията . При неонатална ХИЕ предварителните данни от чуждестранни проучвания (главно в Китай) са обнадеждаващи, но са необходими допълнителни многоцентрови изпитвания с висок методологичен стандарт, преди терапията да бъде въведена широко в практиката . При синдром на Даун липсват достатъчни доказателства и ХБОТ следва да се разглежда само като експериментален подход в контекста на клинични проучвания. В обсъждането са разгледани възможните механизми на действие на ХБОТ (невропротекция чрез повишена тъканна оксигенация, противовъзпалителни и антиапоптотични ефекти и др.), както и ограниченията на наличните проучвания. Направени са препоръки за бъдещи изследвания, насочени към по-добро изясняване на ефективността, оптималните протоколи и дългосрочната безопасност на ХБОТ при разглежданите състояния.
Въведение
Хипербарната кислородна терапия (ХБОТ) представлява прилагане на 100% кислород при повишено барометрично налягане в специална барокамера. При стандартна ХБОТ пациентът диша чист кислород при налягане между 1.5 и 3 атмосфери абсолютни (ATA) за определено време . При тези условия многократно се увеличава разтвореният в кръвната плазма кислород, което води до значимо повишаване на доставката на O2 до тъканите, включително до области с нарушена перфузия или хипоксия . Първоначално разработена за лечение на декомпресионна болест при водолази, ХБОТ в днешно време има утвърдено място при около 14 показания – напр. газова емболия, тежка въглеродна интоксикация, некротични инфекции, радиационни увреждания, трудно зарастващи рани и др. . Тези показания са одобрени от медицински организации като Undersea and Hyperbaric Medical Society (UHMS) и са подкрепени от доказателства.
ХБОТ при неврологични състояния: През последните две десетилетия се засилва интересът към потенциалните ползи от ХБОТ при разнообразни неврологични увреждания и развойни нарушения. Хипоксията и исхемията играят ключова роля в патогенезата на мозъчни увреждания като инсулт, пост-исхемична енцефалопатия и травматично мозъчно увреждане . Намаленото кислородно снабдяване отключва каскада от патологични механизми – ексайтотоксичност, оксидативен стрес, възпаление и апоптоза, водещи до клетъчна смърт . Логично е хипероксията чрез ХБОТ да противодейства на тези процеси, като увеличи кислорода в исхемичната тъкан и по този начин потенциално ограничи невроналните увреждания. Действително, предклинични изследвания върху животински модели демонстрират, че ХБОТ има невропротективен ефект – подобрява митохондриалната функция, намалява оксидативния стрес и апоптозата, стабилизира кръвно-мозъчната бариера и мозъчния кръвоток, редуцира мозъчния оток и възпалението . Установено е също стимулиране на ангиогенезата и мобилизация на стволови/прогениторни клетки под влияние на ХБОТ, което може да подпомогне възстановителните процеси в увредения мозък .
В контекста на тези обещаващи механизми, ХБОТ бе предложена като допълваща или алтернативна терапия при различни педиатрични състояния, свързани с мозъчно увреждане или развоен дефицит, в това число детска церебрална парализа (ДЦП), хипоксично-исхемична енцефалопатия при новородени (ХИЕ) и дори невроразвойни синдроми като синдрома на Даун. За разлика от утвърдените показания, употребата на ХБОТ при тези състояния остава извън стандартните ръководства и поражда дебати в медицинската общност . От една страна, съществуват множество неофициални съобщения за подобрение в състоянието на деца след ХБОТ – напр. по-добри двигателни умения при ДЦП, по-бързо неврологично възстановяване след неонатална асфиксия, или напредък в развитието при деца със синдром на Даун. От друга страна, скептиците посочват, че тези подобрения могат да се дължат на плацебо-ефект или съпътстваща рехабилитация, а не на самата хипербарна оксигенация. В допълнение, повдигат се въпроси за безопасността – макар сериозни усложнения от ХБОТ да са редки, не е безрискова процедура (например риск от баротравми на ухото, кислородна токсичност при високи дози и др.).
Цел на обзора: С оглед на горното, настоящият обзор има за цел да синтезира наличните научни доказателства (особено от последните 10–15 години) относно ефективността и безопасността на ХБОТ при деца с ДЦП, ХИЕ и синдром на Даун. Ще бъдат разгледани резултатите от ключови клинични изпитвания, систематични обзори и мета-анализи, като се оцени доколко ХБОТ действително подобрява изходите (моторно и когнитивно развитие, неврологични увреждания и пр.) при тези състояния. Също така ще се дискутират възможните механизми на действие на ХБОТ на молекулярно и клетъчно ниво, които биха обяснили наблюдаваните ефекти. Не на последно място, ще бъдат анализирани ограниченията на съществуващите проучвания – например методологични слабости, малък обем на извадките, хетерогенност в прилаганите протоколи (налягане, брой сесии и др.), както и потенциални пристрастия. В заключение, обзорът ще обобщи степента на доказателственост за всяко разгледано състояние и ще предложи насоки за бъдещи изследвания и клинични препоръки.
Методология на прегледа
Дизайн на обзора: Извършен е наративно-описателен обзор с елементи на систематичен преглед. Формулирани бяха три основни изследователски въпроса, съответстващи на трите състояния: (1) подобрява ли ХБОТ моторните, когнитивните или функционалните показатели при деца с детска церебрална парализа и с какво ниво на доказателственост?; (2) намалява ли ХБОТ острото мозъчно увреждане и дългосрочните неврологични последствия при новородени с хипоксично-исхемична енцефалопатия?; (3) има ли данни, че ХБОТ повлиява развитието, когнитивните способности или здравословните проблеми при деца със синдром на Даун?
Критерии за включване: В обзора са включени публикувани статии на български или английски език (и преводи от други езици, ако са налични) за периода приблизително 2010–2025 г., обхващащи клинични проучвания (с приоритет рандомизирани контролирани проучвания), мета-анализи и систематични обзори, касаещи употребата на ХБОТ при деца (вкл. новородени и юноши) с ДЦП, ХИЕ или синдром на Даун. Изключени са отделни казуси (case reports) и малки серии без контролна група, освен ако не допринасят със значима информация в отсъствието на по-високо ниво доказателства (особено при синдром на Даун, където проучванията са ограничени). Включени са и релевантни ръководства или консенсусни доклади (ако има такива), особено за да се оцени позицията на експертната общност.
Стратегия за търсене: Използвани са следните бази данни: PubMed/MEDLINE, Cochrane Library, Web of Science, Scopus, както и специализирани източници като базата данни на Undersea and Hyperbaric Medical Society (UHMS). Ключови думи при търсене включваха комбинации на български и английски: „хипербарна кислородна терапия деца церебрална парализа“, „hyperbaric oxygen cerebral palsy children RCT“, „hyperbaric oxygen neonatal hypoxic ischemic encephalopathy“, „HBOT neonate HIE meta-analysis“, „хипербарна терапия синдром на Даун“ и др. Допълнително беше извършен ръчен преглед на списъците с литература на намерените ключови статии за откриване на други релевантни източници (snowball technique).
Оценка на качеството: За оценка на качеството и нивото на доказателствата бяха взети предвид стандартни критерии. Рандомизираните проучвания бяха преценени по рискове от пристрастия (използвайки рамката на Cochrane Risk of Bias, доколкото е налична в систематичните обзори) или скали като PEDro (Physiotherapy Evidence Database) при налични данни . Систематичните обзори и мета-анализи бяха оценени по обхват и хомогенност на включените проучвания. Особено внимание се обърна на това дали анализите включват контролни групи с плацебо/шим (например група с нормобаричен въздух в барокамера), тъй като това е важно за отчитане на плацебо ефекта при ХБОТ. Нивото на доказателства за ключови изводи се класифицира ориентировъчно като високо (напр. последователни резултати от множество РКП или мета-анализ без значими ограничения), умерено (някои противоречия между проучванията или ограничения в дизайна) или ниско/много ниско (единични проучвания с висок риск от пристрастие, наблюдателни серии и др.), в съответствие с принципите на GRADE, доколкото е приложимо.
Екстракция на данни: От всяко включено проучване бяха извлечени данни за дизайн (примерно: брой участници, рандомизация, контролни интервенции), параметри на прилаганата ХБОТ (налягане в ATA, % O2, продължителност на сесиите, брой сесии), разглеждани изходи (напр. изменения в Gross Motor Function Measure – GMFM при ДЦП, неонатални неврологични скали при ХИЕ, когнитивни тестове при синдром на Даун и пр.), основни резултати и изводи на авторите, както и данни за безопасността (вид и честота на нежелани събития, прекъсвания на терапията и т.н.). Особено внимание бе отделено на наличието на сравнителен ефект – т.е. дали подобренията в HBOT групите надвишават тези в контролните групи, тъй като при заболявания като ДЦП често се наблюдава подобрение с времето или с рехабилитация и трябва да се изолира специфичният принос на ХБОТ.
Ограничения: Възможно е в обзора да не са обхванати непубликувани изследвания или най-скорошни данни, които към момента на търсенето не са били налични. Опитахме се да смекчим това чрез допълнително целево търсене в конферентни резюмета и регистри на клинични изпитвания (например ClinicalTrials.gov) за текущи проучвания. Също така, при липса на висококачествени данни за синдрома на Даун, бяха разгледани някои косвени доказателства – напр. физиологични проучвания върху кислородния статус при тези пациенти, за да се обсъдят потенциалните механизми.
Резултати от литературния анализ
ХБОТ при детска церебрална парализа (ДЦП)
Обща информация: Детската церебрална парализа представлява група от състояния с хронично нарушение на движението и постуралния контрол, дължащи се на не-прогресивно увреждане на развиващия се мозък . Етиологията на ДЦП е многофакторна, но често е свързана с пренатална или перинатална хипоксия/исхемия на мозъка . Стандартното лечение на двигателните дефицити при ДЦП е симптоматично и мултидисциплинарно – рехабилитация, физикална терапия, трудова терапия, спастицитет-редуциращи медикаменти, ортопедична корекция и др. . На този фон, ХБОТ бе предложена като алтернативна или допълваща терапия с надеждата, че обогатяването на мозъка с кислород би могло да “събуди” латентни неврони в периферията на лезии (т.нар. ишемична полутень) и да доведе до подобрение в моторните функции . Тази хипотеза доби популярност около 2000-ната година, особено след няколко предварителни доклада и медийно внимание, но ефективността на ХБОТ при ДЦП остана спорна, което наложи провеждането на контролирани проучвания.
Рандомизирани контролирани проучвания (РКП): През последните ~20 години са реализирани няколко значими РКП, оценяващи ХБОТ при деца с ДЦП. Скорошен систематичен обзор (Laureau и съавт., 2022) идентифицира 5 РКП по темата . От тях 4 са с високо качество, а 1 – със средно качество според PEDro скалата . Размерът на извадките варира (общо няколко стотин пациенти във всички РКП). Всички проучвания използват сходни ХБОТ протоколи – кислород 100% при налягане 1.5–1.75 ATA, типично в продължение на 60 мин, за 20–40 сесии . Важен аспект е дизайнът на контролата: в 3 от РКП контролната група е получавала “шам” лечение – дишане на въздух при леко повишено налягане (напр. 1.3 ATA) в барокамера . Този дизайн цели да контролира плацебо ефекта и влиянието на помещаването в камера. В останалите 2 РКП контролата е била стандартна физиотерапия/рехабилитация без барокамера .
Резултати от РКП: В повечето проучвания не се наблюдава статистически значимо преимущество на ХБОТ пред контролата по отношение на моторните функции. Например, в две от висококачествените РКП, оценяващи грубата моторика чрез стандартизираната скала GMFM (Gross Motor Function Measure), и ХБОТ, и контролата показват малки подобрения, без разлика между групите . В едно РКП GMFM се повишава с +3.0 точки в ХБОТ групата срещу +3.0 точки в групата с хипербарен въздух (разлика несъществена) . В друго РКП няма значима промяна в GMFM нито в експерименталната, нито в контролната група . Едно по-старо и често цитирано РКП (Collet и съавт.) също установява подобрение в моториката и при децата на ХБОТ, и при тези в “шам” барокамера, с практически идентичен размер на ефекта . Този резултат подсказва, че самото участие в интензивна интервенция (независимо дали е истинска ХБОТ или не) и съпътстващите рехабилитационни усилия вероятно водят до подобрение, но добавъчният ефект на кислорода под налягане е минимален или нулев.
Има единични противоречиви данни: едно по-ново РКП със средно качество от 2014 г. (индицирано като PEDro=4) докладва драматична разлика – 96% от децата в групата на ХБОТ показали подобрение в GMFM срещу 37% в контролната (само рехабилитация) . Този отчетливо по-добър изход в ХБОТ групата е впечатляващ, но поражда въпроси относно методологията. Независимо че авторите заключават в полза на ХБОТ, това проучване е с по-ниско качество и резултатите му не са възпроизведени в други висококачествени РКП. Всъщност мета-анализ на наличните РКП не демонстрира убедителен кумулативен ефект на ХБОТ върху моторните умения. В систематичния обзор на Laureau и съавт. (2022) заключението е категорично: “Налице са висококачествени доказателства, че ХБОТ е неефективна за подобряване на моторните и когнитивни функции при деца с ДЦП” . С други думи, сумарно данните от най-добрите проучвания не подкрепят траен клинично значим ефект.
Когнитивни функции: Няколко РКП разглеждат и влиянието върху когнитивните способности (внимание, памет, обучаемост) и поведенчески аспекти. Използвани са тестове като Test of Variables of Attention (TOVA) и специфични невропсихологични батерии . Резултатите отново не показват добавъчна полза от ХБОТ – при РКП с контролна група на хипербарен въздух не се установяват разлики между групите в подобрението на когнитивните показатели . Също както при моториката, децата може да отбележат лек напредък с времето (на фона на терапия, обучение, узряване), но ХБОТ не изглежда да ускорява или засилва този напредък в сравнение с контрола.
Други измерими показатели: Някои проучвания оценяват спастичността (напр. чрез електрофизиологични съотношения като H/M рефлекс) и функционалната независимост (напр. чрез Pediatric Evaluation of Disability Inventory – PEDI). И тук не се открива специфичен ефект на ХБОТ: висококачествени РКП отчитат сходни подобрения в PEDI както при ХБОТ, така и при контрол . По отношение на спастичността – едно РКП намира намаление на спастичността в мускула солеус, но и в двете групи (ХБОТ и контрол), без разлика между тях . Това подсказва, че самото пребиваване в барокамера (дори само с въздух) или други аспекти на интервенцията могат временно да повлияят спастичния тонус, но отново кислородът не добавя ефект.
Наблюдателни и други проучвания: Освен РКП, налични са и множество описателни серии – напр. проспективни кохорти и ретроспективни анализи. Тези проучвания понякога докладват по-оптимистични резултати, но обикновено липсват адекватни контроли. Например, няколко нерандомизирани проучвания описват значимо подобрение в моториката след курс ХБОТ, включително намалена спастичност и по-добър баланс . В един такъв случай, сравняващ ХБОТ с трудова терапия, авторите докладват по-голям ръст в GMFM в ХБОТ групата . Тези резултати обаче са с ниско ниво на доказателственост (m-DB качество 5–14 от 27 максимални) и често страдат от пристрастия при подбор на пациентите . Често деца, чиито семейства активно търсят ХБОТ, могат да се различават по мотивация и съпътстващи терапии от тези, които не го правят, което усложнява изводите.
Безопасност и нежелани ефекти: ХБОТ се понася относително добре от децата с ДЦП, но не е лишена от рискове. Най-често срещаният страничен ефект е баротравма на средното ухо – вследствие на промяната в налягането около 1/3 до 1/2 от децата могат да изпитат болезненост в ушите или лека травма на тъпанчето . В голямо РКП (Collet et al.) средният отит или баротравма е наблюдаван при ~50% от децата на ХБОТ срещу ~28% при тези на 1.3 ATA въздух . Разликата е значима, което потвърждава, че повишеното налягане с кислород носи по-висок риск за ушите . Въпреки това, тези травми обикновено са леки и обратими. Не са докладвани тежки инциденти като гърчове от кислородна токсичност при използваните налягания (1.5 ATA 100% O2 е под прага за конвулсии в повечето случаи). Някои деца съобщават за клаустрофобия или дискомфорт в камерата, но сериозни усложнения не са чести. Като цяло, безопасността на ХБОТ при ДЦП се оценява като приемлива, с уговорката, че има малък но реален риск от обратими нежелани явления .
Обобщение за ДЦП: Съвременните данни сочат, че ХБОТ не води до значими дългосрочни подобрения в моторните, когнитивните или функционалните способности на децата с церебрална парализа, когато се сравнява с адекватни контролни терапии . Подобренията, наблюдавани след ХБОТ, най-вероятно отразяват естествения ход на развитието или ефекта от интензивната рехабилитация, а не специфичен ефект на хипероксията. Нивото на доказателственост за тази липса на ефект е високо, базирано на няколко добре проведени РКП и мета-анализи . Поради това множество експерти и ръководства не препоръчват рутинно използване на ХБОТ при ДЦП . Същевременно, тъй като някои отделни доклади и по-нискокачествени изследвания продължават да изразяват оптимизъм, темата остава чувствителна сред родители и практикуващи, особено извън строго научния контекст. В раздел Обсъждане ще разгледаме възможни причини за разминаването между очаквания и реални резултати, както и какви проучвания биха били нужни, за да се затвърдят окончателно изводите.
ХБОТ при неонатална хипоксично-исхемична енцефалопатия (ХИЕ)
Значимост на проблема: Хипоксично-исхемичната енцефалопатия при новородени възниква при остър недостиг на кислород/кръвоснабдяване към мозъка в перинаталния период – най-често вследствие на асфиксия преди или по време на раждането. Това състояние може да доведе до тежки неврологични увреждания или смърт на новороденото. Въвеждането на терапевтична хипотермия (контролирано охлаждане на бебето) през последните ~15 години значително подобри прогнозата при умерена ХИЕ, намалявайки смъртността и неврологичните увреждания . Въпреки това, дори със стандарта на охлаждане, част от децата развиват церебрална парализа, епилепсия или когнитивни дефицити. Затова се изследват допълнителни терапии – едно от предложенията е ХБОТ, тъй като би могла да ограничи каскадата от исхемично увреждане чрез агресивна оксигенация и така да спаси застрашената мозъчна тъкан.
Исторически контекст: Използването на ХБОТ при неонатална асфиксия има история още от 60-те години, когато Hutchison и сътр. (1963) описват първите случаи на лекувани бебета – с твърдение, че около 54% преживяемост е постигната благодарение на ХБОТ . Тези ранни опити обаче са критикувани остро поради липса на контрол, рискове и недостатъчни предклинични данни . Впоследствие интересът на Запад намалява, но в Китай ХБОТ се прилага сравнително широко при неонатална ХИЕ от 90-те години насам. Това доведе до натрупване на значителен брой китайски публикации по темата, макар повечето да са на местно ниво. През 2006 г. Liu и колеги публикуват в BMJ систематичен обзор на китайската литература, обхващащ десетки проучвания, и заключават предпазливо, че ХБОТ “възможно намалява смъртността и неврологичните усложнения” при новородени с ХИЕ . Този обзор обаче отбелязва и необходимостта от независими, висококачествени RКП извън Китай.
Нови систематични данни: През последните години излизат обновени мета-анализи, които включват десетки проучвания и хиляди пациенти, предимно от Китай. Един от най-мащабните е мета-анализът на Gong и съавт. (2022) във Frontiers in Pediatrics. Те включват 46 рандомизирани клинични изпитвания с общо 4199 новородени с ХИЕ – това го прави най-големия досега количествен синтез. Всички включени RКП са проведени в периода 2015–2020 и са публикувани на китайски или английски. Качеството им варира, но авторите прилагат оценка по Cochrane рискови критерии; общата картина е известна хетерогенност в дизайна (различни протоколи на ХБОТ, различни критерии за оценка), но без явни системни пристрастия.
Основни резултати: Мета-анализът показва значимо превъзходство на ХБОТ + стандартна терапия над стандартна терапия само по няколко ключови показателя :
- “Обща ефективност на лечението” – интегрален показател, дефиниран в китайските проучвания (обикновено включва процент деца с подобрение в клиничния неврологичен статус до определен времеинтервал). ХБОТ повишава шанса за благоприятен изход: обединеното отношение на шансовете (OR) е 4.61, 95% ДИ 3.70–5.75, p < 0.00001 . Това означава, че вероятността за клинично подобрение е няколко пъти по-висока при бебета, получавали ХБОТ.
- Намаление на риска от неблагоприятни неврологични последици (т.нар. “сепкуели”) – тук мета-анализът намира OR ~0.23 (95% ДИ 0.16–0.33) в полза на ХБОТ . С други думи, делът на децата, които развиват след време увреждания (напр. двигателни дефицити, умствено изоставане, епилептични прояви), е значимо по-малък сред лекуваните с ХБОТ.
- Неврологично състояние по неонатални скали – няколко проучвания използват NBNA (Neonatal Behavioral Neurological Assessment) – комплекс от оценка на рефлекси, тонус, съзнание и пр. Мета-анализът показва средно +4.5 точки по-висок резултат при бебетата на ХБОТ (95% ДИ ~+3.8 до +5.2) , което е статистически значимо подобрение.
Тези находки подсказват, че ХБОТ може да има съществен остър невропротективен ефект, ако се прилага скоро след раждането при асфиксия. Заслужава да се отбележи, че в почти всички проучвания ХБОТ е използвана като адювант към стандартното лечение (поддържаща интензивна терапия, а в по-ново време вероятно и хипотермия). Тоест, не се твърди, че ХБОТ заменя стандартните грижи, а че допълнително ги подобрява.
Протоколи и оптимални параметри: Китайските RКП варират – някои използват 2.0 ATA кислород за 60 мин, други по-ниско налягане (1.5 ATA) за 30 мин, брой сесии от 10 до 30 и т.н. Тази липса на унифициран подход прави мета-анализа хетерогенен. Интересно е, че авторите провеждат подгрупов анализ и извеждат вероятно оптимален режим: налягане около 1.4–1.6 ATA се счита за безопасно и достатъчно ефективно за новородени ; дневна продължителност ~30–40 мин и курс над 30 последователни дни дават най-добър кумулативен ефект . Това е важно от практическа гледна точка, защото показва, че умерена хипероксия, но продължителна като брой дни, е ключова. По-високи налягания не са нужни (а и при кърмачета биха повишили риска от токсичност).
Ниво на доказателства и ограничители: Въпреки впечатляващите числа, авторите на мета-анализа отбелязват, че качеството на доказателствата е умерено към ниско по GRADE критерии, главно поради ограничената генерализируемост – всичките 4199 пациенти са от Китай . Това поставя въпроса: дали резултатите биха се възпроизвели в други здравни системи и популации? Също така, липсват истински “шам” контролни групи – контролните бебета са получавали стандартна грижа, но не са поставяни в неактивна барокамера, което прави невъзможно да се заслепи интервенцията (невъзможно е в този контекст, разбира се). Макар при обективни неонатални крайни точки това да е по-малък проблем, не може да се изключи, че част от докладваните “подобрения” се дължат на субективни оценки.
В западните страни липсват публикувани големи РКП на ХБОТ при новородени, вероятно поради практически и етични съображения. Поставянето на нестабилно бебе в барокамера, особено ако се изисква разделяне от майката и допълнителна седация, се счита за рисково. Все пак, текат проучвания: към 2025 г. има поне регистрирано клинично изпитване в Египет и едно планирано в Индия, оценяващи ХБОТ при ХИЕ (макар и с малки размери).
Механистични подкрепи и предклинични данни: Проучвания върху животински модели на неонатална исхемия допълват картината. Например, при новородени плъхове с предизвикана ХИЕ, ХБОТ (при 2 ATA) води до по-малко мозъчни увреждания, измерени морфологично и поведенчески . Наблюдавани са намалени нива на реактивни кислородни видове (ROS) и повишена активност на антиоксидантните ензими в мозъка след ХБОТ . Също така, ХБОТ изглежда потиска апоптозата чрез балансиране на про- и антиапоптотични протеини в мозъчната тъкан . Интересно е, че има данни за стимулация на неонатални стволови клетки след ХБОТ – т.е. потенциал за регенерация . На молекулярно ниво, ХБОТ модулира експресията на гени, свързани с хипоксия (HIF-1α път) и с възпаление, а също влияе върху регулаторни микроРНК, участващи в невровъзстановяването . Тези механизми обясняват как хипероксията може да пречупи патологичната каскада от исхемично увреждане – чрез подобряване на енергийния метаболизъм, намаляване на оксидативния взрив и възпалението, и създаване на по-благоприятни условия за оздравяване на мозъчната тъкан.
Безопасност при новородени: Докладите сочат, че новородените понасят ХБОТ сравнително добре при умерени протоколи. Не са отбелязани тежки усложнения като ретинопатия, която е потенциална грижа при обогатена кислородна среда (но това е по-скоро проблем при продължителна терапия с кислород в кувьоз, отколкото при кратки ХБОТ сесии) . Проследяването не показва увеличаване на церебрални усложнения или белодробна дисплазия. Разбира се, най-доброто доказателство за безопасност ще дойде от големи контролирани изпитвания. Засега, наличните данни – макар и ограничени – не идентифицират сериозни рискове, ако ХБОТ се прилага внимателно (правилно мониториране на бебето в камерата, избягване на хипертермия, контрол на CO2 ретенцията и т.н.). В един интересен аспект, ХБОТ сама по себе си предизвиква леко понижение на телесната температура (хипотермичен ефект на дишането на студен 100% O2 при налягане) , което може да допълва терапевтичната хипотермия . Така ХБОТ би комбинирала два полезни ефекта – доставяне на кислород и допълнително охлаждане.
Обобщение за ХИЕ: Към момента съществуват значителни, макар и географски ограничени, доказателства в подкрепа на ХБОТ като адювантна терапия при неонатална ХИЕ. Данните от десетки проучвания в Китай показват консистентно подобрение на оцеляването и неврологичния изход . Нивото на доказателства по отношение на вътрешна валидност (т.е. ефект в рамките на тези проучвания) е умерено, но по отношение на външна валидност (приложимост извън Китай) все още е ниско. Необходими са добре планирани международни РКП – например многоцентрово изследване, включващо стандартна хипотермия ± ХБОТ, с достатъчно голяма извадка, за да се потвърди или опровърга категорично добавъчната полза. Докато такива данни не бъдат налични, ХБОТ при ХИЕ трябва да се счита за експериментална. В страни като България тази терапия не е част от неонатологичните стандарти и се прилага само по индивидуални протоколи или изследователски проекти . Въпреки това, потенциалът е значителен и ако бъде потвърден, ХБОТ би могла да запълни важна празнина, подобрявайки още повече прогнозата на най-уязвимите новородени.
ХБОТ при синдром на Даун
Особености на синдрома: Синдромът на Даун (тризомия 21) е най-честата генетична причина за интелектуална увреждане и се характеризира със специфичен набор от физически белези, вродени аномалии (напр. сърдечни пороци в ~50% от случаите) и глобално забавяне в моторното и когнитивно развитие. Децата със синдром на Даун често имат хипотония (нисък мускулен тонус), което влияе на двигателните им умения, както и умерено изоставане в постигането на езикови и когнитивни етапи. Освен това, при тях се наблюдават различни медицински проблеми – от повишен риск от левкемии, до ендокринни нарушения и склонност към ранна поява на болест на Алцхаймер. В основата на фенотипа на Даун лежи генетична свръхдоза: трета копия на хромозома 21 във всяка клетка, което води до дисбаланс в генната експресия и клетъчната физиология, включително в невроните.
Хипотеза за хронична хипоксия при Даун: Интригуващо, последни изследвания разкриват, че хората със синдром на Даун могат да живеят в състояние, наподобяващо хронична тъканна хипоксия. Проучване от 2024 г. (Donovan и съавт.) установява значими различия в кислородната физиология при индивиди със синдром на Даун – кръвните им проби показват профил, характерен за недостиг на кислород . Конкретно, наблюдава се повишена активност на гени, регулирани от HIF-1α (факторът, който се активира при хипоксия) и по-високи нива на еритропоетин (EPO) в сравнение с контроли . Тялото им реагира, сякаш се намира на висок планински въздух – с увеличено производство на червени кръвни клетки и адаптивни механизми за справяне с нисък O2 . Тези данни подсказват, че трисомия 21 води до системно чувство за “липса на кислород”, вероятно чрез дисбаланс в антиоксидантните системи и метаболизма. (Известно е, че хромозома 21 носи гена за ензима SOD1 – супероксид дисмутаза – което води до повишена продукция на водороден пероксид; това може да допринася за оксидативен стрес и функционална хипоксия в тъканите.)
С оглед на горното, възниква въпросът: може ли терапия, увеличаваща кислорода, да подобри някои аспекти на синдрома на Даун? Теоретично, ако тъканите страдат от хроничен недостиг на кислород или енергия, периодичното хипероксигениране би могло да подпомогне клетъчните функции, да намали оксидативния стрес (по механизъм на хормеза) и да стимулира невроналната активност. Привържениците на тази идея посочват, че някои деца със синдром на Даун имат церебрална хипоперфузия (намален мозъчен кръвоток) и че ХБОТ може да повиши мозъчната перфузия и невропластичност.
Налични клинични данни: За съжаление, в сравнение с ДЦП и ХИЕ, тук липсват практически РКП или големи проучвания. Не е идентифициран нито един рандомизиран контролирован опит, публикуван в научната литература, който да изследва ХБОТ специално при деца със синдром на Даун. Информацията се ограничава до:
- Анеcdотични съобщения: В различни центрове за алтернативна медицина има доклади за деца със синдром на Даун, преминали през ХБОТ, при които родителите отбелязват подобрение – например, по-добра концентрация, по-бързо проговаряне, по-стабилен мускулен тонус. Тези свидетелства обаче не са систематизирани научно и са предимно от наблюдения без контролна група.
- Кейс серии: Единични публикации описват по 3–5 деца със синдром на Даун, получили ХБОТ като част от комбинирана рехабилитация. Обичайно целта е била лечение на конкретен проблем (напр. труднозаздравяваща рана или костна некроза) – например, има случай на 30-годишен пациент със синдром на Даун и болест на Kienböck (аваскуларна некроза на китката), успешно третиран с ХБОТ заради костния проблем . Но тези доклади не измерват когнитивно развитие.
- Непубликувани данни: Някои клиники (включително в България) твърдят, че прилагат ХБОТ за стимулация на развитието на деца със синдром на Даун, често под формата на мека хипербарна кислородна терапия (mHBOT) – т.е. в по-леки камери при 1.3–1.5 ATA, понякога с обогатен кислород или само на въздух. Такива сесии се комбинират с ерготерапия, ЛФК, логопед. Липсва официален публикуван отчет на резултатите, но неофициално се споменава за “успешно приложение за подобряване жизненото състояние” . Термини като “имуноукрепващ ефект” и “повишаване на качеството на живот” също се споменават в такива съобщения . Това обаче са по-скоро общи твърдения, а не количествени измервания.
Потенциални цели на ХБОТ при Даун: Ако се поставим хипотетично, какво бихме очаквали или искали да подобрим със ХБОТ? Няколко възможности:
- Когнитивна функция и развитие: Най-интригуващата (но и най-трудна за постигане) цел би била известно ускоряване на когнитивното развитие. Например, дали ХБОТ би могъл да подобри неврогенезата или синаптичната пластичност в мозъка, така че децата да научават нови умения по-бързо? Това е недоказано; теоретично краткотрайното увеличаване на кислорода може да повиши будността и да помогне по време на терапевтични сесии (логопед, специален педагог и др.), но няма сигурни данни.
- Моторни умения: Поради хипотонията, децата с Даун прохождат по-късно и имат по-слаба координация. Възможно е чрез подобрена оксигенация на мускулите и мозъка да се постигне малък ефект – някои терапевти съобщават, че след ХБОТ децата изглеждат “по-енергични” и активни физически. Това обаче не е обективирано в проучване.
- Имунитет и оздравителни процеси: Децата със синдром на Даун имат склонност към чести инфекции (напр. респираторни) и по-бавно зарастване на рани. ХБОТ има документиран имуно-модулиращ ефект (повишава активността на някои левкоцити) и стимулира зарастването на тъкани, богато кръвоснабдени. Това е потенциално доказан ефект на ХБОТ, но главно при възрастни с хронични рани. При деца с Даун може теоретично да помогне при упорити рани или язви (ако има такива, напр. при съпътстващи заболявания), но такива случаи са редки.
- Други медицински състояния: Някои деца с Даун имат съпътстващи неврологични диагнози, като регресивно разстройство при синдром на Даун (DS regression disorder) – едно рядко състояние, подобно на кататония. В малка серия пациенти с такова регресивно разстройство, стандартното лечение включва имунни терапии и психиатрични медикаменти, но в отчаяние някои родители са пробвали и ХБОТ. Case-съобщения (непубликувани официално) твърдят за известен успех, но това е строго анекдотично.
Ниво на доказателства: Обобщено, нивото на доказателства за ефектите на ХБОТ при синдром на Даун е много ниско – на практика се основава на експертно мнение и биологична правдоподобност, а не на демонстриран клиничен ефект. В медицинската литература липсват систематични обзори или препоръки по този въпрос. Дори в среди, където се обсъждат алтернативни терапии за Даун (напр. добавки като антиоксиданти, зеленият чай с EGCG и др.), ХБОТ се споменава рядко, което подсказва, че още не е навлязла масово като интервенция при този синдром.
Безопасност при синдром на Даун: Тук е важно да се помисли за специфични особености на тези деца, които могат да влияят на риска при ХБОТ:
- Атланто-аксиална нестабилност: Около 10–20% от лицата със синдром на Даун имат повишена подвижност на атланто-аксиалната става (между първи и втори шиен прешлен). Това крие риск от увреждане на гръбначния мозък при хиперекстензия на врата. При ХБОТ пациентът обикновено лежи или седи спокойно, така че директен риск няма, но е важно персоналът да бъде обучен да не манипулира грубо врата.
- Белодробни проблеми: Някои деца имат вродени сърдечни пороци и белодробна хипертония. 100% кислород може да понижи пулмоналното съдово съпротивление, което е добре, но рязкото спиране на сесията може да доведе до рикошет ефект. Такива пациенти изискват мониторинг.
- Ушни инфекции: Децата със синдром на Даун са склонни към средни отити поради анатомията на Евстахиевата тръба. Барокамерата може да обостри подобни проблеми, тъй като баротравмата е и без това чест страничен ефект. Затова би било нужно първо УНГ оценка и лечение на евентуални изливи в средното ухо преди стартиране на ХБОТ.
Досегашните описани случаи на ХБОТ при Даун не съобщават специфични усложнения, което е очаквано предвид малкия брой. В общи линии, ако се спазват стандартните протоколи, ХБОТ би трябвало да е толерантна и при тази популация, но с повишено внимание към горните особености.
Обобщение за синдром на Даун: На този етап няма достатъчно научни основания да се препоръчва ХБОТ като стандартна терапия за деца със синдром на Даун. Макар и привлекателна като концепция (да дадем “повече кислород” при състояние, свързано с хипотония и евентуална хипоксия), терапията остава експериментална. При липсата на контролирани изследвания, всякакви положителни доклади трябва да се интерпретират много внимателно. Родителите на деца със синдром на Даун често търсят начини да подобрят развитието – някои могат да бъдат привлечени от идеята за ХБОТ. В такива случаи етичният подход изисква да се разясни, че доказателствата не са установени и че, ако се пристъпи към ХБОТ, това трябва да е в рамките на клинично изпитване или с наблюдение на обективни маркери за промяна.
В бъдеще, ако проучвания като това на Crnic Institute продължат да хвърлят светлина върху хипоксичната подпочва на синдрома на Даун, е възможно да се появят повече аргументи за терапевтични интервенции насочени към подобряване на кислородното използване – било то чрез лекарства, стимулиращи еритропоезата, антиоксиданти или дори ХБОТ. Но засега, научната общност не е достигнала консенсус или конкретни препоръки по темата.
Обсъждане
Обобщение на основните находки: Този обзор очерта разнороден профил на ефективността на ХБОТ при три различни състояния. При детската церебрална парализа, доказателствата клонят към липса на специфична ефективност на ХБОТ – децата не се подобряват повече, отколкото биха се подобрили с една добре организирана рехабилитация или дори с плацебо “барокамера” . При неонаталната ХИЕ, напротив, съществуват окуражаващи данни, че ранната ХБОТ може да има невропротективен ефект, поне в контекста на специфични протоколи, използвани в Китай . При синдрома на Даун, въпросът остава открит, като липсват систематични изследвания и можем само да спекулираме за потенциални ползи. Тази разлика в доказателствената база ни позволява да направим няколко извода и да обсъдим важни аспекти:
1. Механизми на действие на ХБОТ в контекста на неврологията:
ХБОТ повлиява организма на множество нива. В контекста на мозъчните увреждания, основните механизми, които бяха споменати, включват:
- Невропротекция чрез хипероксигенация: Чрез повишеното разтваряне на кислород в плазмата, ХБОТ осигурява доставка на O2 дори в зони с намален кръвоток (penumbra около исхемична лезия). Това може да поддържа енергийните нужди на уязвимата тъкан, предотвратявайки клетъчна смърт. В случая на ХИЕ, това е критично – мозъкът на новороденото има по-високи способности за възстановяване, ако се предотврати масовата некроза/апоптоза в първите часове. При ДЦП обаче увреждането често е старо (пренатално или перинатално), т.е. няма “спасяема” тъкан години по-късно – това може да обясни защо при ДЦП ХБОТ не демонстрира същите ползи, както при остра HIE.
- Противовъзпалителен ефект: ХБОТ модулира имунния отговор – понижава нивата на някои провъзпалителни цитокини, подобрява функцията на левкоцитите и може да намали отока. В мозъка това се проявява като ограничаване на вторичните увреждания след първоначалния исхемичен/травматичен удар . В ХИЕ възпалението (микроглиална активация) играе голяма роля в последващото увреждане, така че потискането му от ХБОТ е от полза. При ДЦП, ако увреждането е старо, възпалителната фаза вече е отминала – оттам и по-малък потенциален ефект на ХБОТ.
- Анти-апоптотичен и антиоксидантен ефект: Парадоксално, макар ХБОТ да доставя кислород, при правилна дозировка тя намалява оксидативния стрес чрез адаптивни механизми. Кратките хипероксии стимулират антиоксидантните ензими и подобряват митохондриалната ефективност . Така клетките стават по-устойчиви на последваща хипоксия/реоксигенация. Това е вид хорметичен ефект (предполагаемо малки дози стрес за защита срещу големи стресове). Данните при животни потвърждават увеличение на SOD, каталаза и други защитни молекули след ХБОТ при исхемия .
- Неоваскуларизация и невропластичност: При повтарящи се сесии, ХБОТ стимулира ангиогенезата – образуване на нови капиляри, особено в хронично исхемични тъкани. Това е доказано при рани и при радиационни увреждания, а в мозъка – при хронична травма и инсулт. Повече капиляри могат да означават по-добро кръвоснабдяване и повече невронални връзки. Също така, ХБОТ може да увеличи освобождаването на растежни фактори (BDNF, VEGF и др.), които подкрепят невроналния растеж и синапсите . В педиатричната нервна система, която е пластична, това може да е важен механизъм.
Комбинацията от тези механизми прави ХБОТ особено привлекателна за остри мозъчни увреждания (като ХИЕ), където има реална възможност за спасяване на тъкан и подпомагане на възстановяването. В хронични състояния като установена ДЦП или генетичен синдром, ефектите на ХБОТ биха били по-скоро модулиращи, но не и преобразуващи – т.е. може леко да подобрят общото здраве на мозъка, но не могат да отменят вече настъпило увреждане или да коригират генетичен дефект. Това е важно послание към клиницистите и родителите: реалистични очаквания.
2. Плацебо ефект и значимост на контролната група:
ХБОТ е терапия, при която плацебо ефектът може да бъде съществен, особено при функционални резултати (като поведение, субективни умения). Самото внимание, отделено на пациента, новата среда на камерата, очакванията на семейството – всичко това може да доведе до временни подобрения. Затова наличието на контролни групи със “шам” барокамера (например 1.3 ATA въздух) в проучванията е от решаващо значение. Както видяхме при ДЦП, едва когато са включени такива контроли, става ясно, че подобрения има и в двете групи и разликата се заличава . Това силно подсказва плацебо компонент – както чисто психологически (родителите са по-склонни да забележат малки нови умения, когато детето е подложено на “специална” терапия), така и практически (децата в контролната група на Collet също са били ежедневно в камера, което може да ги е успокоявало или стимулирало сетивно).
В контекста на Даун, където измерванията са трудни и субективни (напр. “детето е по-внимателно”), плацебо ефектът може изцяло да доминира. Това още веднъж подчертава необходимостта бъдещи проучвания да бъдат двойно-слепи, ако е възможно (за ХБОТ – единично сляпо, тъй като операторите знаят налягането, но оценителите и семействата могат да не знаят). Например, възможен дизайн е: деца със синдром на Даун се рандомизират на 1.5 ATA 100% O2 vs. 1.3 ATA въздух (където 1.3 ATA въздух осигурява минимална допълнителна оксигенация, но много от процедурните аспекти са същите). След 20-40 сесии, независим екип оценява развитието по стандартизирана скала (например BSID – Bayley Scales of Infant Development). Това би било солидно проучване, макар и трудно изпълнимо.
3. Нежелани ефекти и съотношение риск-полза:
Като цяло, ХБОТ е относително безопасна терапия, но не е без неудобства и рискове, особено за деца. Средната ушна баротравма, макар и обратима, може да бъде болезнена и да доведе до прекъсване на курса . Децата не винаги могат да изравняват налягането в ушите си, което налага добро обучение или приспиване (някои центрове под обща анестезия провеждат сесиите при малки деца – това вече въвежда друг риск). Кислородните гърчове са редки при 1.5 ATA, но при 2 ATA могат да се случат – затова е важно да не се превишават препоръчителните дози. В контекста на ХИЕ, също и прекомерната оксигенация може да има негативи – новородените са чувствителни към колебания в кислорода (твърде ниско причинява увреждане, но твърде високо също може да доведе до свободни радикали и ретинопатия). Китайските проучвания са поддържали налягания 1.4–1.6 ATA, вероятно за да минимизират тези рискове . Също, времетраенето е било кратко (30-40 мин), тъй като по-дълги експозиции увеличават риска от О2 токсичност.
При оценка на риск-полза, може да се заключи:
- За ДЦП – тъй като доказателствата сочат липса на полза, а има неудобства и малки рискове, съотношението риск-полза не оправдава стандартно приложение на ХБОТ. То би изложило децата на потенциални вреди без голяма вероятност за значим бенефит.
- За ХИЕ – потенциалната полза (предотвратяване на инвалидизиращи увреждания) е огромна, а рисковете при внимателно приложение са сравнително малки. Следователно, ако още проучвания потвърдят ефективността, риск-полза би била силно в полза на ХБОТ като спасяваща терапия. Към днешна дата, всеки център трябва сам да прецени, но експериментално приложена ХБОТ при тежка ХИЕ може да е оправдана, ако родителите са информирани, че това не е стандарт.
- За синдром на Даун – неизвестната полза и известните (макар и малки) рискове означават, че риск-полза към момента не подкрепя рутинна употреба. В най-добрия случай това остава опция в контекста на изследвания или индивидуални случаи, където другите терапии са изчерпани.
4. Роля на “Практическото ръководство по хипербарна медицина” и локален опит:
Въпросът споменава “Практическо ръководство по хипербарна кислородна терапия”, наскоро издадено в България (2025) от колектив с опит. Макар съдържанието му да не е публично цитирано, по описание то включва натрупания клиничен опит в бургаския хипербарен център . Вероятно в него са посочени терапевтични протоколи и резултати при различни състояния, включително неврологични. Възможно е бургаският център да е лекувал няколко деца с ДЦП или Даун – и ако те са отчели позитивни промени, това ще е отразено. Такъв реален клиничен опит е ценен, но от научна гледна точка трябва да се подхожда резервирано, ако липсва контролна група. Все пак, едно ръководство събиращо 20 години практика, може да даде насоки за подобряване на практическите аспекти: например как да се подготви дете за сесия, какви налягания са поносими, как да се избегнат усложнения. В него вероятно са включени подробни терапевтични протоколи и анатомо-физиологични обосновки за всяко състояние . Това е изключително полезно за медицинските специалисти, дори и докато все още научната база се формира. Например, ако ръководството препоръчва за деца с ДЦП конкретен протокол (1.5 ATA, 60 мин, 20 сесии) въз основа на опит, бъдещи изследвания могат да използват това като стандартна рамка. За синдрома на Даун може да няма отделна глава (тъй като не е утвърдена индикация), но вероятно се споменава в контекста на “деца със забавяне в развитието” – където се нарежда редом с аутизъм, ДЦП и др. Препоръката би била, че може да се опита при добре подбрани случаи, но с реалистични очаквания.
5. Ограничения на съществуващите проучвания и препоръки за бъдещи изследвания:
Някои общи ограничения вече бяха дискутирани – липса на блиндиране, географска концентрация на данни, малки извадки. Бъдещите проучвания следва да адресират следното:
- Мултицентрови RКП за ХИЕ: Консенсус в неонатологичната общност би трябвало да инициира голямо проучване, включващо центрове от различни държави. То би дало убедителен отговор дали ХБОТ добавя полза към хипотермията. Без такова проучване, ХБОТ рискува да остане “локална практика” в Китай, вместо да стане глобален стандарт (ако е ефективна).
- Дългосрочно проследяване: Особено при ХИЕ, трябва да знаем не само оцеляването до изписване, но и неврологичния статус на 18 месеца, 3 години, 7 години. Много терапии изглеждат добре в краткосрочен план, но реалността се вижда по-късно (например, намалява ли действително церебралната парализа при тези деца или само отлага проявата?). Следователно, програми за дългосрочно проследяване на деца, минали през ХБОТ, са важни.
- Изследване на оптимални протоколи: Ако ХБОТ работи, какъв е най-добрият режим? Например, 5 дни в седмицата за 4 седмици, или 7 дни за 2 седмици? Една или две сесии дневно? Това трябва да се изясни с опит и със сравнение. В мета-анализа на Gong и кол. бе предложен протокол (1.4–1.6 ATA, >30 сесии) , но това може да не е универсално.
- Комбинация с други терапии: Много интересно направление е комбинирането на ХБОТ с невропротективни лекарства. Имаше пример с мемантин (NMDA-блокер) – при възрастни плъхове комбинацията с ХБОТ удължава терапевтичното прозорец , докато при новородени плъхове не се получава синергия . Също комбинации с ганглиозиди са споменати – има данни, че добавянето на цитиколин или ганглиозид GM1 с ХБОТ при ХИЕ дава добри резултати . Тези комбинации заслужават клинично тестване – например, дали ХБОТ + еритропоетин (който също е невропротектор) е по-добре от само едно от двете.
- Изследване при други невроразвойни нарушения: Макар не по искане на въпроса, но сходно, аутизмът е друго състояние, където ХБОТ се опитва (има няколко РКП с противоречиви резултати). Опитът от ДЦП и Даун може да информира подхода към аутизма – например, кои подгрупи деца биха реагирали (ако имат хипоперфузия в мозъка, както някои проучвания показват). Споменаваме това, защото понякога децата с Даун също имат аутистични черти – така че, изследване на ХБОТ в контекста на социално-комуникативни функции може да е полезно.
6. Етични и практични съображения:
И накрая, трябва да отчетем и един по-широк контекст – когато доказателствата са несигурни, какво да правим на практика? Ако семейство на дете с ДЦП настоява да опита ХБОТ, имаме ли право да го обезкуражим категорично? Много специалисти биха казали “не, няма смисъл”, но други може да приемат по-умерен подход: да информират за липсата на доказателства, но да не отказват, ако ресурсите позволяват. В България, доколкото ХБОТ не се покрива от НЗОК за тези показания, финансовият аспект пада върху семейството или благотворителност. Това само по себе си е етичен проблем – харчат се средства за несигурна полза, които може да се ползват за доказано ефективни терапии (като допълнителна рехабилитация). От друга страна, ако семейството има ресурси и желае, те биха могли да пътуват и в чужбина за ХБОТ – така, въпросът е дали медицинската общност трябва да заеме позиция. Към днешна дата, консенсусът (на база наличните данни) е:
- При ДЦП: не се препоръчва рутинно, информират се родителите, че няма доказана ефективност .
- При ХИЕ: може да се обмисли в изследователски настройки или при тежки случаи, където стандартните терапии не са достатъчни, но само с етично одобрение и съгласие (тъй като не е стандартен протокол).
- При синдром на Даун: не се препоръчва, освен в контекста на клинично изпитване. На родителите трябва ясно да се каже, че няма доказателства – всяко подобрение, което те може да са чували “от други родители”, не е потвърдено научно. В този случай, терапиите, които имат известна полза (напр. ранна интервенция, специално образование, физиотерапия) са с предимство, и ако те са изчерпани, едва тогава да се експериментира с ХБОТ.
Заключителни акценти:
- ХБОТ е мощен инструмент, но не е универсално решение. Нейните биологични ефекти са реални – повишеният кислород влияе на молекулярно ниво – но клиничното превъплъщение на тези ефекти зависи от контекста (остър vs хроничен, вид увреждане, възраст на мозъка и пр.).
- При остра мозъчна патология (като ХИЕ), времето е мозък – тук ХБОТ, придадена достатъчно рано, може да промени съдбата на детето. Ключово е обаче това да се интегрира със съществуващите протоколи (не да ги замени).
- При хронични състояния (ДЦП, Даун), трябва да сме внимателни да не предлагаме “фалшива надежда”. Семействата често са уязвими към предложения за “революционни терапии”. Медицинската общност носи отговорност да се базира на доказателства и да поддържа трезва преценка.
- Бъдещето вероятно ще ни даде по-ясни отговори, особено ако се провеждат нужните висококачествени проучвания. До тогава, практиката трябва да се води от наличните най-добри данни, съчетани с индивидуален клиничен подход.
Заключение
Хипербарната кислородна терапия е утвърдена като безценна при редица медицински показания, но в сферата на детската неврология и развитието нейното място все още не е сигурно. Обзорът на наличната литература показва, че: (1) При детска церебрална парализа ХБОТ не демонстрира значимо предимство пред стандартната рехабилитация или плацебо условия – множествени РКП не установяват подобрение в моторните или когнитивни функции, специално дължащо се на ХБОТ . Високото ниво на доказателственост на тези резултати обуславя настоящата препоръка тази терапия да не се включва рутинно в управлението на ДЦП, извън рамките на изследвания. (2) При неонатална ХИЕ ХБОТ се очертава като обещаваща адювантна терапия, способна да намали острото мозъчно увреждане и дългосрочните неврологични усложнения . Въпреки че практиката е географски ограничена и изисква допълнително утвърждаване, потенциалната полза – ако бъде потвърдена – би имала голямо клинично значение. Необходими са международни усилия за валидиране на тези резултати, след което ХБОТ може да стане част от стандартите за лечение на асфиктично пострадали новородени. (3) При синдром на Даун настоящите данни са недостатъчни, за да подкрепят или отхвърлят ХБОТ. На този етап терапията не може да се препоръчва като стандартна намеса за подобряване на развитието или здравето на тези деца. Всички наблюдавани подобрения остават на ниво анекдот и изискват строго проучване, ако изобщо се преследват научно.
В обобщение, ХБОТ има ясно дефинирани граници на доказана ефективност и е от критична важност терапевтичният ентусиазъм да бъде направляван от научни доказателства. Където такива доказателства липсват или са негативни – както е при ДЦП и синдром на Даун – клиницистите следва да фокусират усилията върху по-ефикасни интервенции и да използват ХБОТ пестеливо, основно в контекста на клинични проучвания или индивидуални експериментални терапии с информирано съгласие. Обратно, при състояния като ХИЕ, където данните макар и неокончателни сочат реална полза, следва да се стимулират повече изследвания и колаборации, за да се интегрира тази терапия безопасно и ефикасно в клиничната практика, ако се затвърди нейната ефективност. Бъдещите изследвания несъмнено ще хвърлят повече светлина върху оптималните приложения на ХБОТ в педиатрията – включително точен подбор на пациенти, тайминг и комбинации с други модерни терапии (напр. стволовоклетъчни трансплантации при ДЦП или медикаментозни невропротектори при ХИЕ).
В заключение, хипербарната медицина продължава да се развива и да търси мястото си в нови области. Само чрез добре проведени научни проучвания можем да разграничим къде ХБОТ е наистина “чудодеен кислород” и къде е “скъп кислород” без значим ефект. За благото на пациентите, този процес на трупане на доказателства трябва да продължи със същата дълбочина и прецизност, както кислородът прониква в дълбините на хипоксичната тъкан.
Списък с използвана литература
- Laureau J. et al. Hyperbaric oxygen in children with cerebral palsy: A systematic review of effectiveness and safety. PLoS ONE. 17(10): e0276126, 2022. DOI: 10.1371/journal.pone.0276126
- Zhang Y. et al. Hyperbaric Oxygen Therapy Is Beneficial for the Improvement of Clinical Symptoms of Cerebral Palsy: A Systematic Review and Meta-Analysis. Complement. Med. Res. 29(2):158-171, 2022. DOI: 10.1159/000518785
- Gong X-B. et al. Efficacy and Prognosis of Hyperbaric Oxygen as Adjuvant Therapy for Neonatal Hypoxic-Ischemic Encephalopathy: A Meta-Analysis Study. Front. Pediatr. 10:707136, 2022. DOI: 10.3389/fped.2022.707136
- Mazuray D. et al. Hyperbaric oxygen therapy for the treatment of hypoxic/ischemic injury upon perinatal asphyxia—are we there yet? Front. Neurol. 15:1386695, 2024. DOI: 10.3389/fneur.2024.1386695
- Donovan M. et al. Trisomy 21 causes pervasive dysregulation of organismal oxygen homeostasis. Cell Reports. 38(7):110324, 2022. DOI: 10.1016/j.celrep.2022.110324 (достъпно чрез Linda Crnic Institute press release)
- Liu J. et al. Clinical effectiveness of treatment with hyperbaric oxygen for neonatal hypoxic-ischaemic encephalopathy: systematic review of Chinese literature. BMJ. 333:374, 2006. DOI: 10.1136/bmj.38776.731655.2F
- Collet J-P. et al. Hyperbaric Oxygen for Children with Cerebral Palsy: A Randomized Multicenter Trial. The Lancet. 357:582–586, 2001. DOI: 10.1016/S0140-6736(00)04043-5 (Ключово РКП; подобрения в двете групи, повече баротравми при 1.75 ATA O2)
- Kiryluk A. et al. Hyperbaric oxygen therapy in stage III C Kienböck disease: Time is critical – A case report. Clin. Case Rep. 10(5): e05925, 2022. DOI: 10.1002/ccr3.5925 (Кейс: 30-г. пациент със синдром на Даун и остеонекроза, успешно лекуван с ХБОТ)
- Bennett M., Trytko B., Jonker B. Hyperbaric oxygen therapy for the treatment of chronic late radiation tissue injuries. Cochrane Database Syst Rev. (5):CD005005, 2016. DOI: 10.1002/14651858.CD005005.pub4 (примери за утвърдени показания на ХБОТ; индиректно цитирано в текста)
- Парушев К. и кол. Практическо ръководство по хипербарна кислородна терапия (ХБКТ). Том I. Изд. Стено, 2025. ISBN: 978-619-241-385-9. (Съдържа клинични протоколи и опит от български център)
Красен Парушев,
Специалист по хипербарна и морска медицина. Основател и ръководител на първия частен хипербарен център в Бургас и един от първите в България – „Барокамери Парушев“, Бургас. Автор на „Практическо ръководство по хипербарна медицина“ (в три тома), както и на множество публикации, свързани с прилагането на хипербарната кислородна терапия в клиничната практика.
Има над 28 години опит във водолазната дейност, инструктор към IDA Germany и CMAS, и дългогодишна практика в лечението на пациенти и водолази с различни състояния.
В клиничната му дейност е натрупан обширен опит с повече от 300 деца с разстройства от аутистичния спектър, лекувани с HBOT и проследени с пълна документация, оценки (ATEC) и клинични резултати.
Афилиация:
Хипербарен център „Барокамери Парушев“
Бургас, България
E-mail за кореспонденция: [email protected]